- Přehledy IS
- APS (20)
- BPM - procesní řízení (22)
- Cloud computing (IaaS) (10)
- Cloud computing (SaaS) (33)
- CRM (51)
- DMS/ECM - správa dokumentů (20)
- EAM (17)
- Ekonomické systémy (68)
- ERP (77)
- HRM (27)
- ITSM (6)
- MES (32)
- Řízení výroby (36)
- WMS (30)
- Dodavatelé IT služeb a řešení
- Datová centra (25)
- Dodavatelé CAD/CAM/PLM/BIM... (39)
- Dodavatelé CRM (33)
- Dodavatelé DW-BI (50)
- Dodavatelé ERP (71)
- Informační bezpečnost (50)
- IT řešení pro logistiku (45)
- IT řešení pro stavebnictví (25)
- Řešení pro veřejný a státní sektor (27)
 ERP systémy
ERP systémy CRM systémy
CRM systémy Plánování a řízení výroby
Plánování a řízení výroby AI a Business Intelligence
AI a Business Intelligence DMS/ECM - Správa dokumentů
DMS/ECM - Správa dokumentů HRM/HCM - Řízení lidských zdrojů
HRM/HCM - Řízení lidských zdrojů EAM/CMMS - Správa majetku a údržby
EAM/CMMS - Správa majetku a údržby Účetní a ekonomické systémy
Účetní a ekonomické systémy ITSM (ITIL) - Řízení IT
ITSM (ITIL) - Řízení IT Cloud a virtualizace IT
Cloud a virtualizace IT IT Security
IT Security Logistika, řízení skladů, WMS
Logistika, řízení skladů, WMS IT právo
IT právo GIS - geografické informační systémy
GIS - geografické informační systémy Projektové řízení
Projektové řízení Trendy ICT
Trendy ICT E-commerce B2B/B2C
E-commerce B2B/B2C CAD/CAM/CAE/PLM/3D tisk
CAD/CAM/CAE/PLM/3D tisk | |
| Přihlaste se k odběru newsletteru SystemNEWS, který každý týden přináší výběr článků z oblasti podnikové informatiky | |
 | |
Technologický informační systém ve farmacii
Specifika monitorování a řízení výrobního procesu
 Farmaceutická výroba je specifická důrazem na vysokou kvalitu a stabilitu výsledného produktu stejně jako celého výrobního procesu. Veškeré postupy musí odpovídat regulatorním požadavkům autorizovaného orgánu státního dozoru, v České republice se jedná o Státní ústav pro kontrolu léčiv (SÚKL). Tato organizace zároveň vykonává dozor nad dodržováním svých nařízení.
Farmaceutická výroba je specifická důrazem na vysokou kvalitu a stabilitu výsledného produktu stejně jako celého výrobního procesu. Veškeré postupy musí odpovídat regulatorním požadavkům autorizovaného orgánu státního dozoru, v České republice se jedná o Státní ústav pro kontrolu léčiv (SÚKL). Tato organizace zároveň vykonává dozor nad dodržováním svých nařízení.


Pro dosažení shody s požadavky musí veškeré procesy odpovídat doporučení tzv. správné výrobní praxe (SVP), v angličtině good manufacturing practices (GMP). Pro jednotlivé aspekty farmaceutické výroby pak existují souhrny příslušných pravidel komplexně označované zkratkou vycházející z anglické terminologie GxP (pro jednotlivé dotčené oblasti je pak x nahrazeno příslušnou zkratkou). Obecně přijatým standardem pro návrh, implementaci, používání a dokumentaci informačních systémů ve farmacii je pak GAMP (Good Automated Manufacturing Practices). Tento standard obsahuje kompletní popis postupů a dokumentace související s automatizací procesů ve farmacii a zahrnuje celý cyklus od počáteční rozvahy až po odstavení vysloužilého systému.
Základním požadavkem na IS ve SVP regulované oblasti je to, že jeho zavedení nesmí vést ke snížení jakosti výrobků, kontroly procesů, jištění procesů a nemělo by docházet k nárůstu celkového rizika v procesu. Zásadní rozdíl oproti klasickému projektu IS spočívá v potřebě systém od začátku navrhovat jako validovatelný. Validace je ve své podstatě zdokumentování, že IS plní účel, kvůli kterému byl zaveden, jeho výsledky jsou opakovatelné a očekávatelné a splňuje regulatorní požadavky. Aby byl systém validovaný, musí proces jeho návrhu a validace odpovídat tzv. V – diagramu.
Pro jednotlivé fáze pak vznikají příslušné dokumenty:
- User requirements specification – specifikace uživatelských požadavků
- Functional specification – funkční specifikace
- Design specification – specifikace návrhu
V rámci validace jsou pak prováděny jednotlivé testy. IQ – instalační kvalifikace ověřuje a dokumentuje, že je systém proveden dle specifikace návrhu. OQ – operační kvalifikace ověřuje a dokumentuje, že systém plní požadované funkce a PQ – výkonnostní kvalifikace, ověřuje, že zavedením informačního systému se výrobní procesy nezpomalili.
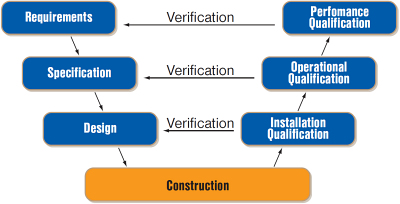
V-diagram
Shrnutí validačního procesu dle GAMP
- Cílem validace je ověřit, že použitý SW odpovídá požadavkům, sběr dat probíhá bez problémů, uložené hodnoty odpovídají skutečnosti a pravdivě se zaznamenají do reportu. V jednotlivých bodech zkušebního scénáře je podrobně popsáno, co a jakým způsobem má být testováno.
- Validátor prochází jednotlivé body a po provedení testu vyznačí, zda byl test úspěšný,
- a zaznamená případné nálezy.
- Každý testovaný bod je zároveň nutné zdokumentovat otiskem obrazovky, výpisem z databáze, případně jiným způsobem, který dokládá, že byl test proveden a s jakým výsledkem.
- V případě nesrovnalostí je validátor povinen informovat příslušné pracovníky a je třeba určit, zda jde o kritickou chybu a kdo je za ni zodpovědný. Po opravě je třeba znovu projít všechny kroky validace, které s nálezem souvisí.
- Součástí validace však není pouze kontrola sběru a zobrazení dat, ale i ověření verze
- a nastavení použitého hardwaru a kontrola související dokumentace, která zahrnuje například kalibrační listy jednotlivých měřicích čidel nebo existenci SOP (z anglického Standard Operating Procedure), což je dokument popisující daný výrobní proces nebo postup, a který je pro každý výrobní postup nebo proces vyžadován.
- Validační testy jsou v závěru shrnuty do validační zprávy, která zahrnuje všechny důležité informace o testovaném procesu jako například definici procesu, jména osob zodpovědných za jednotlivé části projektu, odkaz na protokol validace, seznam testů a jejich zpracování
- a vyhodnocení, použité definice a zkratky, celkový závěr, zda projekt splňuje požadavky uvedené v protokolu validace, a popřípadě doporučená nápravná opatření či poznatky.
Technologický informační systém
Pro online monitoring, vizualizaci, archivaci a reporting procesních a dalších dat určených pro podporu řízení technologických procesů používáme soubor softwarových nástrojů, který nazýváme technologický informační systém (dále TIS).
Cílem implementace TIS je vytvoření jednotné platformy pro monitorování procesních veličin, tj. ukládání procesních dat, vizualizace systémů a dokumentace procesů, zajištění snadné dostupnosti aktuálních procesních dat důležitých pro rozhodování ve výrobě při vynaložení minimálního úsilí na jejich sběr, zajištění dokumentace procesů ve výrobě, čehož je dosaženo ukládáním a využitím historických dat do databáze, zajištění elektronického monitoringu podpůrných systémů, sledování trendů monitorovaných veličin a jak už vyplývá z textu výše i validace systému TIS a jeho následné udržování ve validovaném stavu.
Vstupem dat TISu jsou různé řídicí systémy na úrovni PLC nebo i speciální systémy s vlastní řídicí jednotkou. Tyto vstupy se standardně sjednotí na úrovni OPC serveru (dle https://opcfoundation.org/). Přenos mezi OPC serverem a sběračem probíhá převážně asynchronně, to umožňuje minimální vytížení koncového zařízení při získání častého vzorkování dat pro více OPC klientů. Obvyklá perioda vzorkování pro farmacii se pohybuje 1–10 s. Data z OPC serveru jsou ukládána do databáze přes sběrače (archivátory), např. SCADA systém. Pro možný výpadek síťové komunikace je u sběrače implementován systém kruhového bufferu, který zajišťuje po obnovení síťového výpadku uložení nasbíraných dat do centrální databáze. Sběrač se umísťuje co nejblíže k OPC serveru (zdroji) tak, aby se eliminovala případná ztráta dat.
Přínosy TIS ve farmacii
1. Zdokumentování výrobního procesu
- Průběžné sledování monitorovaných veličin a porovnávání s požadovanými limity
- Průkaznost a dokladovatelnost při auditech – dlouhodobá archivace pro účely SÚKL, pro účely kontroly kvality, opakovanosti výrobních parametrů, dohledání výrobních parametrů při reklamaci
- Rychlá dohledatelnost informací pro řešení nestandardních situací (rychlé vyloučení kontrolovatelných vlivů)
- Využití předdefinovaných reportů jako přílohy operačních listů
- Sledování trendů
2. Úspora práce a nákladů
- Včasná identifikace problémů a chyb v monitorovaných oblastech a díky tomu i ušetření nákladů spojených s jejich následky a odstraňováním
- Snížení potřeby ručních přenosů tabulek, grafů, reportů z měření
- Eliminace rizika chyby při získávání, přenosu a zpracování údajů z měření
3. Podpora standardů
Databáze, reporting, vizualizace a alarmy
Nejčastěji se používají buď relační SQL nebo pak pro větší objemy dat realtime databáze, např. PI od firmy OSIsoft. Realtime databáze mají v sobě integrován komprimační algoritmus využitelný pro sběr analogových veličin, který výrazně uspoří ukládané místo. Realtime databáze jsou vhodné pro úsporné ukládání velkého množství dat (až desetitisíce sbíraných veličin), ale hlavně pro rychlost jejich získání. Uložená data jsou následně reportována nástroji, které uživatelé běžně používají, jako například Excel nebo BI reportig.
Reporting může probíhat různými způsoby. Nejrozšířenějšími jsou ale dva typy. První typ reportů si uživatel vytvoří na požádání, když je potřebuje (buď podle šablony, nebo vlastním dotazem do databáze přes speciální Excel add-in doplněk) a druhý typ reportů se vytváří dle předpřipravené šablony v určitém definovaném čase, nebo po ukončení výrobního procesu. Pracovat s takto vytvořenými reporty pak uživatel může dle své potřeby. Podstatou reportingu ve farmacii je přesné dokládání výrobního procesu dle času a výrobní šarže.
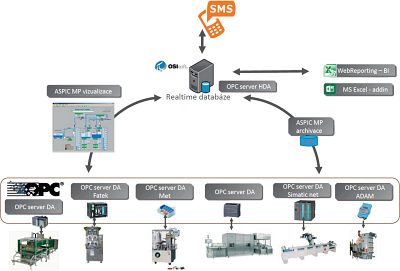
Pro vizualizaci výrobních procesů se využívá SCADA aplikace v konfiguraci klient – server. Vytvořená vizualizace běží na serveru a uživatelé k ní mají přístup na klientských obrazovkách, kde vidí vizualizační obrazovky jednotlivých procesů s vyznačením sběrných míst. V SCADA aplikaci je pak možné vytvořit graf z online hodnot, ale i z historických hodnot z centrální databáze.
Všechna nasbíraná online data je možné vyhodnocovat i pomocí alarmů (notifikací), kdy se vyhodnocují jednotlivé mezní veličiny. Pokud dojde k překročení meze, spustí se ve vizualizaci alarm
a hlášení odejde zodpovědnému pracovníkovi formou SMS či e-mailu. Jednotlivé alarmy je možné potvrzovat tak, aby byla zaznamenána reakce obsluhy. Ve farmacii se standardně monitoruje prostředí (např. přetlaky, částicová čistota, teplota, vlhkost) a stavy technologií (výroba vody, teploty v různých zařízení, průběhy mycích procesů atd.).
 |
Ing. Leoš Pfannenstiel Autor článku působí ve společnosti Merz. |
 |
Ing. Lea Poštolková Spoluautorka článku působí ve společnosti Merz. |


| Po | Út | St | Čt | Pá | So | Ne |
| 1 | 2 | 3 | ||||
| 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 |
| 18 | 19 | 20 | 21 | 22 | 23 | 24 |
| 25 | 26 | 27 | 28 | 29 | 30 | 31 |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 18.5. | Konference ISSS 2026 |
| 19.5. | TechEd |
| 19.5. | Webinář FLEXI IT | Novinky & Tipy & Triky 2021... |
| 21.5. | Online konference Kyber bez keců |
| 21.5. | ManageEngine Meetup 2026 Bratislava |
Formulář pro přidání akce
| 4.6. | Setkání zákazníků a partnerů ABIA CZ & dFlex 2026... |




















